(Tổ Quốc) - Về công văn đề nghị thay thế thuốc gây tê tủy sống Bupivacaine WPW Spinal 0,5% Heavy (của Ba Lan), lãnh đạo Sở Y tế Cần Thơ khẳng định đã gửi từ hồi tháng 4/2019 còn Cục Quản lý Dược (Bộ Y tế) lại cho rằng mình chưa hề nhận được.
- 23.11.2019 Cục Quản lý Dược khẳng định chưa nhận được báo cáo đề nghị dừng sử dụng thuốc gây tê từ Sở Y tế Cần Thơ
- 22.11.2019 Nhiều tỉnh thành đã phản ánh về chất lượng thuốc gây mê tủy sống đến Cục Quản lý Dược rất lâu trước vụ 2 sản phụ ở Đà Nẵng tử vong
- 20.11.2019 Sự cố y khoa tại Bệnh viện Phụ nữ Đà Nẵng: Bộ Y tế vào cuộc
- 20.11.2019 Vụ sản phụ tử vong, nguy kịch sau khi sinh mổ: Tạm dừng sử dụng thuốc gây tê của Ba Lan sản xuất
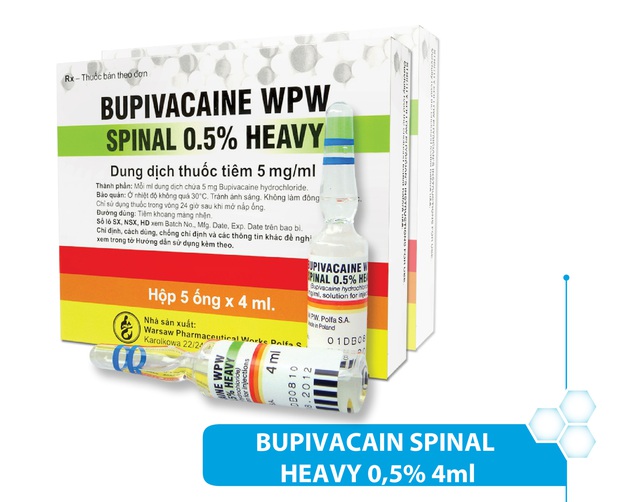
Thuốc gây tê tủy sống Bupivacaine WPW Spinal 0,5% Heavy (của Ba Lan) nghi là nguyên nhân khiến 2 sản phụ tử vong, 1 sản phụ nguy kịch ở Đà Nẵng.
Sau khi vụ việc 2 sản phụ tử vong, 1 sản phụ nguy kịch tại Bệnh viện Phụ nữ Đà Nẵng nghi do dùng thế thuốc gây tê tủy sống Bupivacaine WPW Spinal 0,5% Heavy (của Ba Lan) làm xôn xao dư luận mấy ngày qua, nhiều tỉnh, thành phố trên cả nước cũng đã lên tiếng về loại thuốc này.
Ông Phạm Quốc Tuấn, Phó Giám đốc Sở Y tế tỉnh Bến Tre trả lời trên Báo Pháp luật TP.Hồ Chí Minh, đầu năm 2019, sau khi sử dụng loại thuốc này có một ca bị sốc thuốc dẫn đến tử vong, Hội đồng chuyên môn của bệnh viện, Sở Y tế đều kết luận do sốc thuốc gây tê trên. Sở Y tế Bến Tre cũng đã báo cáo ngay sự cố về Cục quản lý dược (Bộ Y tế).
Ông Tuấn còn cho hay, thời điểm này Sở Y tế tỉnh Bến Tre cũng có công văn triển khai tất cả đơn vị y tế trong toàn tỉnh ngưng ngay việc sử dụng loại thuốc gây tê do Ba Lan sản xuất.
Tiếp đó, Sở Y tế Cần Thơ đã chủ động gửi công văn đề xuất thay thế thuốc gây tê tủy sống Bupivacaine WPW Spinal 0,5% Heavy (của Ba Lan) sau khi tổng hợp các thông tin từ bệnh viện và Hội Gây mê Đồng bằng Sông Cửu Long.
Nói với Báo Tuổi trẻ, bác sĩ Trần Huỳnh Đào - Trưởng khoa Gây mê hồi sức Bệnh viện Đa khoa Trung ương Cần Thơ, thành viên chi hội Gây mê hồi sức Đồng bằng Sông Cửu Long khẳng định: Sở Y tế Cần Thơ đã gửi công văn đến Cục Quản lý Dược và đơn vị cung cấp thuốc ngưng sử dụng loại thuốc này.
Nội dung này cũng được Phó Giám đốc Sở Y tế Cần Thơ Nguyễn Phước Tồn trả lời trên Báo Giao thông. Theo đó, ông Tồn khẳng định, sau khi nghe tiếp nhận ý kiến các bác sĩ đề đạt về thông tin nguy cơ biến chứng do thuốc gây tê mới, tháng 4/2019, Sở Y tế Cần Thơ đã có công văn về việc thay thế thuốc trúng thầu, loại dùng gây tê tủy sống, từ thuốc do Ba Lan sản xuất sang loại do Pháp sản xuất.

Công văn của Cục Quản lý Dược (Bộ Y tế).
"Văn bản của Sở Y tế Cần Thơ được gửi tới cả Công ty cổ phần dược phẩm Trung ương CPC1 và Cục quản lý dược, Bộ Y tế từ tháng 4/2019. Tuy nhiên, đến nay vẫn chưa nhận được phúc đáp từ phía Bộ Y tế" – ông Tồn cho hay.
Nếu đúng như lãnh đạo Sở Y tế Cần Thơ nói thì quả thật, là một cơ quan quản lý nhà nước về lĩnh vực thuốc nhưng Cục Quản lý Dược (Bộ Y tế) đã quá vô trách nhiệm khi không có sự vào cuộc, sự cảnh báo nào để người dân được biết. Giả sử, nếu Cục Quản lý Dược có cảnh báo kịp thời từ thời điểm đó, có khi, 2 sản phụ ở Đã Nẵng đã không chết đau đơn như vậy.
Tuy nhiên, ngày 22/11, sau khi có những phản ánh từ báo chí, Cục Quản lý Dược (Bộ Y tế) đã chính thức lên tiếng bằng một công văn mang dấu "Khẩn" gửi Sở Y tế Cần Thơ. Công văn do Phó Cục trưởng Cục Quản lý Dược Nguyễn Tất Đạt ký đã khẳng định rằng, giai đoạn từ tháng 4/2019 đến nay, Cục này chưa hề nhận được văn bản nào của Sở Y tế Cần Thơ liên quan đến việc thay thế thuốc như lãnh đạo Sở Y tế trả lời trên báo chí.
Để tránh "gây hiểu lầm cho dư luận", Cục Quản lý Dược (Bộ Y tế) đã đề nghị Giám đốc Sở Y tế Cần Thơ báo cáo cụ thể việc lãnh đạo Sở Y tế Cần Thơ trả lời trên báo chí. Trong ngày 25/11, Sở Y tế Cần Thơ phải trả lời vấn đề này cho Quản lý Dược bằng văn bản.
Cùng một vấn đề nhưng hai cơ quan quản lý nhà nước về lĩnh vực y tế "người nói ngược, kẻ nói xuôi". Dư luận đang hết sức băn khoăn, liệu, công văn yêu cầu thay thế thuốc gây tê của Sở Y tế Cần Thơ có thật hay không và nếu có thật thì được Sở này gửi đến Cục Quản lý Dược bằng con đường nào? Trong vấn đề này, Cục Quản lý Dược và Sở Y tế Cần Thơ ai nói thật, ai nói dối?





